
Además de los químicos y la radiación, las mutaciones también pueden venir de los virus. Los virus son "organismos" muy pequeños que pueden infectar las células de otros animales o plantas. Los humanos son susceptibles a un gran número de infecciones virales. Estos patógenos no son iguales a las bacterias a pesar del hecho de que ambos pueden causar enfermedades humanas. Es más, los tratamientos que curan las infecciones bacterianas no son útiles en el tratamiento de las infecciones virales. La gripe (el virus de la influenza) y el virus que causa el SIDA (el virus de inmunodeficiencia humana - VIH) son ejemplos comunes de las enfermedades virales.
Los virus pueden trastornar el comportamiento de la célula de varias maneras.
- Pueden causar daño directo al ADN (mutaciones) al insertar sus propios genomas dentro del ADN de la célula huésped. La integración puede interrumpir la secuencia de genes reguladores importantes.
- Los genes virales pueden alterar la regulación celular. Este proceso puede ser de beneficio al virus si le permite la producción rápida de descendientes pero puede ser seriamente dañino a la célula huésped.
- Algunos virus contienen versiones modificadas de genes que han recogido de otras células huésped. Estos genes alterados ya no funcionan adecuadamente, y cuando se introducen en una nueva célula huésped, pueden provocar cierta desregulación y pueden resultar en crecimiento cancerígeno.
A través de sus actividades mutagénicas o de sus efectos en el comportamiento celular, los virus desempeñan un papel muy importante en el desarrollo de ciertos tipos de cáncer en varios animales, incluyendo a los humanos.
Los virus también han sido un enfoque importante en las investigaciones científicas del cáncer. Algunas de las primeras investigaciones sobre la identificación de los oncogenes y los supresores tumorales emplearon a los virus.
Los virus pueden clasificarse dentro de dos categorías: aquéllos que tienen usan al ADN como su material genético y aquéllos que usan ARN como su material genético. Ambos tipos de virus se han asociado con diferentes tipos de cáncer. Puede encontrar más información sobre los temas discutidos en esta página en mayoría de los textos introductorios de biología; nosotros recomendamos Campbell Biology, 11ma edición.1 Los virus conocidos por causar cánceres humanos son:
- Virus de Epstein-Barr (VEB) - linfoma de Burkitt
- Virus de la hepatitis B (VHB) - cáncer de hígado
- Virus de la hepatitis C (VHC) - cáncer de hígado
- Virus del sarcoma de Kaposi (VHH-8)
- Virus del papiloma humano (VPH) - cáncer cervical, de cabeza y cuello, anal, oral, faríngeo y de pene
- Virus linfotrópico humano de células T - tipo 1 (VLHT-1) - leucemia de células T en adultos
- Poliomavirus de células de Merkel - cáncer de piel (carcinoma de células de Merkel)
Virus de Epstein-Barr (VEB) - linfoma de Burkitt2, 3
Cáncer asociado: Enfermedad linfoproliferativa, comúnmente conocida como el linfoma de Burkitt. La cantidad de evidencia que indica que este virus también está relacionado con el linfoma de Hodgkin ha crecido bastante en los últimos años.
Prevalencia: Se estima que más de un 90% de la población mundial está infectada con el virus de Epstein Barr, pues es el patógeno que causa la mononucleosis infecciosa (la "enfermedad del beso")
Transmisión: El mecanismo de transmisión es generalmente desconocido, posiblemente a través de la saliva.
Infección: La infección con el virus de Epstein Barr usualmente comienza en las células epiteliales de la orofaringe, la nasofaringe posterior y las glándulas paratiroides. Partiendo de ahí, este virus infecta a las células B y establece una infección persistente. Casi todas las infecciones con el virus de Epstein Barr son controladas por el sistema inmunológico y las personas infectadas son asintomáticas (no tienen síntomas de la infección).
Potencial cancerígeno: La infección de las células B es necesaria para la carcinogénesis mediada por el virus de Epstein-Barr. Sin embargo, el porcentaje de infecciones que resultan en el cáncer es pequeño, pues la mayoría de casos se observan en personas inmunocomprometidas o con trasplantes. Estos pacientes se ven más vulnerables a esta progresión de la infección ya que carecen de una actividad inmunológica suficientemente competente para inhibir el crecimiento de las células B infectadas. La carcinogénesis mediada por este virus parece ser el resultado de la actividad del material genético viral. Se presume que la actividad de ciertas proteínas es primordial en la inmortalización de la célula B: las proteínas latentes de la membrana del virus y antígeno nuclear del virus. La proteína latente de la membrana 1 se introduce dentro la membrana de la célula huésped y actúa como un receptor de factor de crecimiento activado, resultando en el crecimiento celular sin regulación. Por otro lado, los antígenos nucleares afectan a las células mediante varios mecanismos, por ejemplo, pueden alterar la actividad de los genes de supresión de tumores, como el Rb, p53, y el Arf.
Lea más sobre el linfoma de Burkitt
Hepatitis B - cáncer de hígado2, 4
Cáncer asociado: Carcinoma hepatocelular humano
Prevalencia: Las hepatitis B es una enfermedad infecciosa común a nivel mundial, sin embargo su incidencia es particularmente alta en la región subsahariana de África y en el sureste de Asia. Se estima que más de 400 millones de personas están infectadas con este virus alrededor del mundo.
Transmisión: La hepatitis B se transmite a través del contacto con sangre contaminada, sudor o lágrimas. También puede transmitirse a través de contacto sexual y de la madre a feto.
Infección: La infección con la hepatitis B ocurre principalmente en el hígado, pero los antígenos virales pueden detectarse en la sangre a través de todo el cuerpo. Una infección crónica se demuestra con la presencia de antígenos virales en la sangre durante más de 6 meses. La infección crónica puede provocar la cirrosis hepática y el desarrollo del cáncer de hígado.
Potencial cancerígeno: 70-85% de los cánceres primarios del hígado surgen de la hepatitis (B y C). La introducción del ADN viral al genoma huésped es un indicador común de los casos de infección hepática crónica y en cáncer. Esto sugiere que juega un papel importante en la carcinogénesis. El ADN del virus codifica una proteína (HBX) que parece promover la proliferación celular e interferir con la reparación del ADN. Se presume que la la carcinogénesis mediada por la hepatitis B se debe a varios factores; por ejemplo, las propiedades oncogénicas de la proteína HBX, el deterioro hepático crónico, la inflamación crónica, y la regeneración de tejido continua que ocurre para reparar los efectos de una infección.
Hepatitis C (VHC) - cáncer de hígado2, 5
Cáncer asociado: Carcinoma hepatocelular humano
Prevalencia: Las hepatitis C es una enfermedad infecciosa común a nivel mundial, sin embargo su incidencia es particularmente alta en la región subsahariana de África y en el sureste de Asia. Se estima que mundialmente más de 170 millones de personas están infectadas con la hepatitis C.
Transmisión: El cáncer de hígado se transmite principalmente a través del contacto de sangre a sangre.
Infección: La hepatitis C ocurre principalmente en el hígado y produce una inflamación más severa que la hepatitis B. Más del 80% de los infectados con la hepatitis C terminan padeciendo de la cirrosis hepática o del mismo cáncer del hígado.
Potencial cancerígeno: La hepatitis B y C son responsables del 70-85% de los cánceres primarios del hígado. A diferencia de la hepatitis B, el virus de la hepatitis C no suele introducir su material genético dentro del genoma del huésped. Varios estudios in vitro han demostrado que la hepatitis C puede afectar a una gran variedad de mecanismos celulares que pueden promover la carcinogénesis, sin embargo estos resultados no se han podido reproducir en estudios in vivo. El potencial cancerígeno de la hepatitis C se debe a su habilidad de causar lesiones hepático al estimular reacciones inmunológicas crónicas, la inflamación y la regeneración de tejidos.
Herpesvirus humano 8 - Sarcoma de Kaposi2, 6
Cáncer asociado: El herpesvirus humano 8 (HVH8) principalmente causa el sarcoma de Kaposi, un tipo de cáncer que afecta la piel y los órganos blandos. HVH8 también está asociado con varios desórdenes sanguíneos.
Prevalencia: El HVH8 es poco común, y sólo 1 a 5% de las personas en Norte América y en el norte de Europa están infectadas. Las poblaciones mediterráneas tienen una tasa de infección más alta (5-20%) y la región subsahariana de África tiene la más alta tasa (>60%). En los Estados Unidos, los hombres homosexuales también tienen una tasa de infección elevada (~40%).
Transmisión: Comúnmente, el HVH8 se transmite a través del contacto sexual o la saliva. La transmisión también puede ocurrir a través de un trasplante de órganos o una transfusión de sangre.
Infección: El HVH8 infecta a las células B, las células epiteliales y posiblemente a los monocitos. La infección con el HVH8 es alta en poblaciones con alta incidencia del Sarcoma de Kaposi y baja en poblaciones con baja incidencia de Sarcoma de Kaposi.
Potencial cancerígeno: A todos los pacientes que padecen del sarcoma de Kaposi se les detecta la presencia del ADN del HVH8, sin embargo la infección con HVH8 en sí no es suficiente para causar el cáncer. El mecanismo exacto por el cual el HVH8 induce el cáncer todavía está bajo investigación. Se presume que el desarrollo del sarcoma de Kaposi comienza como un proceso inflamatorio en el cual las células circulantes (incluyendo las células infectadas con el HVH8) son reclutadas, resultando en más inflamación, daño a los tejidos e infección viral. Entonces, el HVH8 establece una infección persistente la cual puede enviar señales promoviendo angiogénesis e inflamación. Este ciclo puede resultar al final en desarrollo tumoral. Un SIDA no tratado otorga un riesgo 20000 veces más alto de desarrollar el sarcoma de Kaposi. Sin embargo, además de la supresión inmune, el papel del SIDA en el desarrollo del sarcoma de Kaposi aún no se define.

Sarcoma de Kaposi - Imagen del NCI
Virus del papiloma humano (VPH) - cáncer cervical y otros, incluyendo cáncer de cabeza y cuello, anal, oral, faríngeo y de pene
¿Qué es el virus del papiloma humano (VPH)?
Existen más de 200 cepas conocidas del virus del papiloma humano, cada una con su genotipo único. Algunas cepas del virus son responsables por el crecimiento de verrugas comunes o plantares (verrugas en la planta de los pies). Otras cepas pueden infectar el revestimiento interior del cuello uterino, y se clasifican según el riesgo que imponen. Las cepas de alto riesgo son aquéllas que están vinculadas con el cáncer cervical; por ejemplo, las cepas 16 y 18 parecen causar 70% de los casos. Por otro lado, las cepas 6 y 11 son de bajo riesgo y están asociadas con un gran porcentaje de casos de verrugas genitales. 7
Con excepción de la aparición de verrugas genitales, la infección con el virus del papiloma humano es asintomática (no tiene síntomas). En la mayoría de los casos, el VPH no causa ningún problema adicional después eliminado por el sistema inmunológico. 8
Prevalencia
En un estudio estadounidense del 2007 aproximadamente 26.8% de todas las mujeres examinadas (de 14 a 59 años de edad) estaban infectadas con el virus del papiloma humano. Es importante indicar que la mayoría de las infecciones con el VPH se curan dentro de dos años (muchas infecciones no son para toda la vida).9
- 14-19 ~ 24.5%
- 20-24 ~ 44.8%
- 25-29 ~ 27.4%
- 30-39 ~ 27.5%
- 40-49 ~ 25.2%
- 50-59 ~ 19.6%
Transmisión
El virus del papiloma humano se transmite por medio de contacto de piel a piel. Las relaciones sexuales no son necesarias para la transmisión, sin embargo es la ruta más común. El virus puede infectar a las regiones genitales, anales y orales. La infección ocurre cuando los virus penetran una pequeña ruptura en la piel o en las membranas mucosas. La probabilidad de adquirir el VPH en un solo encuentro sexual se desconoce, pero se presume que es alta.10
Verrugas genitales
Algunas cepas del VPH pueden causar el crecimiento de verrugas sobre o alrededor de los genitales o el ano. Las cepas que causan la mayoría de estos casos de verrugas genitales son las cepas 6 y 11. Estos tipos son cepas de bajo riesgo y no están asociadas con cáncer cervical.
Cáncer cervical
El virus del papiloma humano es el factor de riesgo más importante en el desarrollo del cáncer cervical. El virus es responsable de al menos el 90% de los casos. El tipo 16 de alto riesgo de VPH es tipo más común de alto riesgo y es encontrado en más del 50% de los cánceres cervicales. El segundo tipo más común de alto riesgo es el 18 y es responsable del 10-12% de los cánceres cervicales. A pesar de que VPH es responsable de prácticamente todos los casos de cáncer cervical, el 80% de las mujeres se cura de la infección dentro de 1-2 años.
Existen tres pasos necesarios para el desarrollo de cáncer cervical11:
- Infección del VPH. La infección con el VPH es muy común; un estudio reciente estima que más del 26% de las mujeres en los Estados Unidos están infectadas.
- Persistencia del VPH. La persistencia es poco común. En la mayoría de los mujeres (~80%), las infecciones del VPH se curan o se suprimen a causa del sistema inmunológico dentro de 1 a 2 años de exposición. Por lo tanto, la mayoría de los casos de infecciones del VPH NO causan el cáncer cervical. Si la infección del VPH no se cura y persiste por un periodo largo de tiempo, se la neoplasia cervical intraepitelial se puede desarrollar. A seguir se encuentra más información acerca de esta enfermedad.
- Transformación celular e invasión. Esta transformación es poco frecuente en comparación con el número de mujeres que contraen el VPH. La invasión usualmente ocurre después de un largo periodo de infección. Se presume que la displasia severa no ocurre sin la presencia de ciertos cofactores (por ejemplo: fumar, co-infección de VIH, inmunosupresión)
Otros tipos de cáncer
La relación entre el VPH y el cáncer cervical se ya ha estudiado a profundidad por varios años, no obstante existe la posibilidad de que este virus tenga efectos adicionales relacionados al cáncer. Varios estudios recientes demuestran que existe un vínculo sólido entre el VPH con los cánceres de vulva, pene, canal anal, y de cabeza y cuello.12
- 73% de los tumores en la cavidad oral dieron resultados positivos para la presencia del ADN del VPH-16.13
- 80% de los cánceres anales dieron resultados positivos para la presencia del ADN del VPH-16 o 18.
Un estudio poblacional (epidemiológico) del 2012 demostró que existe una relación entre los subtipos de VPH que infectan la piel (llamadas enfermedades cutáneas) y el desarrollo de cáncer de piel de células escamosas. El papel que desempeña el virus dentro del desarrollo de la enfermedad aún no se define clarificado.14
Aprenda más sobre las vacunas del VPH
Aprenda más sobre el cáncer cervical
Cómo el VPH puede causar el cáncer
El VPH invade la piel o la mucosa al entrar por pequeñas roturas en la superficie (incluso aquéllas no visibles a simple vista). Una vez adentro, el VPH infecta las células epiteliales del huésped, engañándolas para que produzcan nuevos virus. En el proceso de reemplazo de las células normales, las células infectadas se desprenden y secretan partículas virales. Las cepas de alto riesgo del VPH pueden introducir su ADN viral dentro del genoma huésped, no obstante, esto no es una parte normal del ciclo de vida de VPH. La integración viral le puede dar a las células huésped infectadas una ventaja selectiva, alargando la duración de la infección. Mientras más tiempo dure la infección, más tiempo tiene el cáncer para desarrollarse.15
A partir de este proceso de integración genética, los genes virales E6 y E7 se pueden sobreexpresar. Las proteínas que producen estos genes habilitan el desarrollo del cáncer. Las proteínas E6 y E7 previenen la actividad de los genes clave de supresión tumoral. Por ejemplo, la proteína E6 inhibe la actividad de la p53, una proteína que controla las reacciones a varios tipos de estrés celular como los defectos en el ADN y las infecciones virales. Asimismo, la proteína E7 inhibe la actividad de la Rb, una proteína que puede prevenir la división celular al bloquear la actividad de los factores de transcripción. Los efectos combinados de estas proteínas ponen a las células en riesgo de llevar a cabo una división descontrolada que puede resultar en cáncer.16, 17
El genoma de VPH contiene muchos genes que codifican la producción de proteínas. [1] Tres de estos genes, E2, E6 y E7, son de interés particular por sus papeles en el desarrollo de cáncer cervical. La proteína E2 se adhiere a las proteínas E6 y E7 para desactivarlas y prevenir su actividad dentro de la célula.[2] Cuando la E6 no está unida a la E2, puede unirse a la p53, y como resultado, la p53 se desintegra. La p53 es una proteína clave en el control del ciclo celular. Se ha observado que la actividad de esta proteína es deficiente en más del 50% de todos los cánceres humanos. Sin la proteína p53, una célula puede continuar dividiéndose aun cuando está dañada. [3] La proteína E6 también causa la expresión de la telomerasa [4], una proteína que se produce bajo condiciones normales en los adultos humanos. La telomerasa mantiene conserva las parte extremas de los cromosomas, previniendo su desintegración y promoviendo así la división continua de las células cancerígenas.[5]
La E7 es otra proteína del VPH que también desempeña un papel crucial el control viral de las células infectadas. Cuando no está unida a la E2, la E7 se adhiere a la proteína Rb e inhibe su actividad normal. Bajo condiciones normales la, Rb se une al E2F, un factor de transcripción que causa progresión del ciclo celular. Como resultado, el E2F no puede llevar acabo su deber como factor de transcripción, y la división celular no ocurre. Por ende, si la E7 se adhiere a la Rb, unión entre la Rb y la E2F no ocurre, y el E2F actúa factor de transcripción. En esencia, la E7 inhibe a un inhibidor de la división celular. Cuando una célula produce la proteína E7, el factor de transcripción E2F causa que la célula se divida, lo cual es un paso crítico en el desarrollo de cáncer. [6] Las proteínas E6 y E7 le ayudan al VPH a tomar control de la división celular e impulsan el desarrollo de cáncer.
¿Podrá el VPH prevenir el cáncer?
Los virus del papiloma humano pueden causar el cáncer, pero también podrían PROTEGER al cuerpo en contra del cáncer. Varias investigaciones realizadas con ratones indicaron que la infección con cierto tipo de VPH (beta-VPH) produjo una respuesta inmunológica en contra del cáncer de piel de células escamosas. Los expertos presumen que la reacción inmune en contra del virus de alguna manera le protege al cuerpo en contra de los cánceres que resultan de la exposición a la radiación ultravioleta. Hoy en día se investiga la posibilidad de utilizar la vacuna del VPH para proteger al cuerpo en contra del cáncer de piel.
Virus linfotrópico humano de células T - tipo 1 (VLHT-1) - leucemia de células T en adultos2, 18
Cáncer asociado: Leucemia de células T del adulto (LLTA)
Prevalencia: Aproximadamente 10 a 20 millones de personas están infectadas a nivel mundial. El VLHT-1 es endémico en el suroeste de Japón, en las islas del Caribe, y en partes de África central y Sudamérica.
Transmisión: El VLHT-1 puede transmitirse a través del contacto sexual o a través de la sangre. Este virus también puede transmitirse a través de la leche materna de la madre al bebé.
Infección: El VLHT-1 es un virus de ARN (un retrovirus) que puede infectar a los linfocitos B y T, a los monocitos y a los fibroblastos.
Potencial cancerígeno: 3 a 5% de las personas con VLHT-1 desarrollan la leucemia de célula T del adulto; la mayoría de los casos se presentan personas de edad mediana. Se presume que por lo menos una de las proteínas reguladoras del VLHT-1 está involucrada en el desarrollo de la LLTA. Por ejemplo, es probable que la proteína Tax contribuya a la carcinogénesis al inducir la proliferación celular, activar las proteínas de supervivencia celular y al promover la inestabilidad cromosómica.19, 20
Muchos otros retrovirus también están asociados con el cáncer, por lo cual el uso de vectores retrovirales en el tratamiento del cáncer debe realizarse con consciencia de la posibilidad de que surjan problemas mayores. 21, 22
Poliomavirus de células de Merkel - cáncer de piel (carcinoma de células de Merkel)
Las células de Merkel están ubicadas en la capa externa de la piel (la epidermis) y su función exacta aún se desconoce. Sin embargo parecen estar involucradas en la percepción sensorial (como detectar las texturas).23, 24
El poliomavirus de las células de Merkel ha sido asociado con un tipo de cáncer de piel que las afecta: el carcinoma de las células de Merkel.25 Las causas de este tipo de cáncer aún no se logran determinar. Por otro lado, las posibles relaciones del carcinoma de las células de Merkel con otros tipos de cáncer de piel (el carcinoma de las células escamosas y el carcinoma de las células basales) se encuentran bajo investigación.26, 27
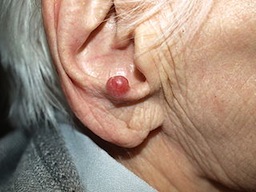
Las siguientes imágenes, de la derecha a la izquierda, ilustran un tumor de las células de Merkel, una célula de Merkel vista por debajo un microscopio, y las partículas virales del poliomavirus de Merkel.


- 1 Urry, L. A., Cain, M. L., Wasserman, S. A., Minorsky, P. V., & Reece, J. B. (2017). Campbell Biology (11th ed.). Pearson.
- 2abcde E. Boccardo and LL Villa. Viral Origins of Human Cancer. Current Medicinal Chemistry. 2007; 24: 2526-39. [PUBMED]
- 3 Brady G, Macarthur GJ, Farrell PJ. Epstein-Barr virus and Burkitt lymphoma. Postgrad Med J. 2008 Jul;84(993):372-7. [PUBMED]
- 4 Lupberger J, Hildt E. Hepatitis B virus-induced oncogenesis. World J Gastroenterol. 2007 Jan 7;13(1):74-81. [PUBMED]
- 5 Castello G, Scala S, Palmieri G, Curley SA, Izzo F. HCV-related hepatocellular carcinoma: From chronic inflammation to cancer. Clin Immunol. 2010 Mar;134(3):237-50. Epub 2009 Nov 11. [PUBMED]
- 6 B. Ensoli, C. Sgadari, et al. Biology of Kaposi's sarcoma. European Journal of Cancer. 2001; 37: 1251-1269. [PUBMED]
- 7 Schiffman M, Castle PE, Jeronimo J, Rodriguez AC, Wacholder S. "Human papillomavirus and cervical cancer." Lancet. 2007 Sep 8;370(9590):890-907. Review. [PUBMED]
- 8 zur Hausen H. Papillomaviruses and cancer: from basic studies to clinical application. Nature Reviews. Cancer. 2002; 2(5):342-50 [PUBMED]
- 9 Dunne EF, Unger ER, Sternberg M, McQuillan G, Swan DC, Patel SS, Markowitz LE. Prevalence of HPV infection among females in the United States. JAMA. 2007;297(8):813-9. [PUBMED]
- 10 Burchell AN, Winer RL, de Sanjosé S, Franco EL. Chapter 6: Epidemiology and transmission dynamics of genital HPV infection. Vaccine. 2006 Aug 31;24 Suppl 3:S3/52-61. Epub 2006 Jun 2. [PUBMED]
- 11 Schiffman M, Castle PE. Human papillomavirus: epidemiology and public health. Archives of Pathology and Laboratory Medicine. 2003; 127(8):930-4. [PUBMED]
- 12 Chaturvedi AK. Beyond cervical cancer: burden of other HPV-related cancers among men and women. J Adolesc Health. 2010 Apr;46(4 Suppl):S20-6. [PUBMED]
- 13 D'Souza G, Kreimer AR, Viscidi R, Pawlita M, Fakhry C, Koch WM, Westra WH, Gillison ML. Case-control study of human papillomavirus and oropharyngeal cancer. New England Journal of Medicine. 2007;356(19):1944-56. [PUBMED]
- 14 Iannacone MR, Gheit T, Waterboer T, Giuliano AR, Messina JL, Fenske NA, Cherpelis BS, Sondak VK, Roetzheim RG, Michael KM, Tommasino M, Pawlita M, Rollison DE. Case-control study of cutaneous human papillomaviruses in squamous cell carcinomas of the skin. Cancer Epidemiol Biomarkers Prev. 2012 Jun 15. [Epub ahead of print] [PUBMED]
- 15 Hamid NA, Brown C, Gaston K. The regulation of cell proliferation by the papillomavirus early proteins. Cell Mol Life Sci. 2009 May;66(10):1700-17. [PUBMED]
- 16 Jabbar S, Strati K, Shin MK, Pitot HC, Lambert PF. Human papillomavirus type 16 E6 and E7 oncoproteins act synergistically to cause head and neck cancer in mice. Virology. 2010 Aug 24. [Epub ahead of print] [PUBMED]
- 17 Moody CA, Laimins LA. Human papillomavirus oncoproteins: pathways to transformation. Nat Rev Cancer. 2010 Aug;10(8):550-60. Epub 2010 Jul 1. [PUBMED]
- 18 Masao Matsuoka and Kuan-Teh Jeang. Human T-Cell Leukemia Virus Type I at Age 25: A Progress Report. Cancer Research. 2005; 65(11):4467-70. [PUBMED]
- 19 Boxus M, Willems L. Mechanisms of HTLV-1 persistence and transformation. Br J Cancer. 2009 Nov 3;101(9):1497-501. Epub 2009 Sep 29. [PUBMED]
- 20 Chlichlia K, Khazaie K. HTLV-1 Tax: Linking transformation, DNA damage and apoptotic T-cell death. Chem Biol Interact. 2010 Nov 5;188(2):359-65. Epub 2010 Jun 15. [PUBMED]
- 21 Nair V. Retrovirus-induced oncogenesis and safety of retroviral vectors. Curr Opin Mol Ther. 2008 Oct;10(5):431-8. [PUBMED]
- 22 Ruprecht K, Mayer J, Sauter M, Roemer K, Mueller-Lantzsch N. Endogenous retroviruses and cancer. Cell Mol Life Sci. 2008 Nov;65(21):3366-82. [PUBMED]
- 23 Moll I, Roessler M, Brandner JM, Eispert AC, Houdek P, Moll R. Human Merkel cells--aspects of cell biology, distribution and functions. Eur J Cell Biol. 2005 Mar;84(2-3):259-71. [PUBMED]
- 24 Maricich SM, Morrison KM, Mathes EL, Brewer BM. Rodents rely on Merkel cells for texture discrimination tasks. J Neurosci. 2012 Mar 7;32(10):3296-300. [PUBMED]
- 25 Chang Y, Moore PS. Merkel cell carcinoma: a virus-induced human cancer. Annu Rev Pathol. 2012 7:123-44. Epub 2011 Sep 13. [PUBMED]
- 26 Ganzenmueller T, Yakushko Y, Kluba J, Henke-Gendo C, Gutzmer R, Schulz TF. Next-generation sequencing fails to identify human virus sequences in cutaneous squamous cell carcinoma Int J Cancer. 2012 Apr 5. doi: 10.1002/ijc.27581. [Epub ahead of print] [PUBMED]
- 27 Rollison DE, Giuliano AR, Messina JL, Fenske NA, Cherpelis BS, Sondak VK, Roetzheim RG, Iannacone MR, Michael KM, Gheit T, Waterboer T, Tommasino M, Pawlita M. Case-control study of Merkel cell polyomavirus infection and cutaneous squamous cell carcinoma. Cancer Epidemiol Biomarkers Prev. 2012 Jan;21(1):74-81. Epub 2011 Oct 20. [PUBMED]
