¿De dónde salen los medicamentos nuevos? ¿Por qué toma tanto tiempo en que se aprueben medicamentos nuevos? ¿Por qué son tan caros los medicamentos?
¿De dónde salen los medicamentos nuevos? ¿Por qué toma tanto tiempo en que se aprueben medicamentos nuevos? ¿Por qué son tan caros los medicamentos?
Todas estas preguntas son validas y las contestaciones pueden ser encontradas en esta página sobre el descubrimiento y desarrollo de medicamentos.
- Una Historia Breve del Descubrimiento y Desarrollo de Medicamentos
- ¿De Dónde Vienen los Medicamentos?
- Pros y Contras de los Fármacos Naturales y Sintéticos
- Ejemplos de Medicamentos de Cáncer
- Buscando Medicamentos Posibles
- Examinando con Precausión los Posibles Medicamentos
- Optimización y Pruebas Pre-Clínicas
- Solicitudes para Nueva Droga de Investigación (IND)
- Ensayos Clínicos
- Solicitud para un Nuevo Medicamento (NDA)
- Posterior a la Aprobación: Fabricación y Más Investigación
- Aspectos Financieros del Desarrollo y Venta de Medicamentos
Una Historia Breve del Descubrimiento y Desarrollo de Medicamentos
Las escrituras más antiguas sobre el uso de medicamentos son como del 2500 aC. Debajo encontrarás un cronograma breve del uso de medicamentos.
- Circa 2500 aC
- Pen T'Sao - Libro chino por el Emperador Shen Nung sobre raices y gramas medicinales.1
Pen T'Sao
- 1550 aC
- Ebers Papyrus - Colección de 800 prescripciones para el uso de plantas medicinales como ajo, sauce, enebro, aloe y muchas más.1

Ebers Papyrus
- Antes del siglo 20
- Los medicamentos se hacían de extractos crudos y semi-puros de plantas, animales, microbios y minerales.2
- Siglo 20
- La teoría de receptores de medicamentos concluyó que químicos en los extractos son responsables por la actividad biológica del medicamento. Esta teoría ayudó a decifrar las estructuras químicas de ingredientes activos en los extractos naturales, lo cual llevó al desarrollo de la química sintética.3
- Los científicos empiezan a usar bases no naturales (sintéticas y semi-sintéticas) para el desarrollo y descubrimiento de medicamentos.2
- Adviento de tecnologías nuevas y revolucionarias para el descubrimiento y desarrollo de compuestos terapéuticos posibles, como técnicas de separación automatizada, cribado de alto rendimiento y química combinatoria.4, 5
Fuentes de Fármacos
Los medicamentos que ingerimos, inyectamos e inhalamos frecuentemente con compuestos terapéuticos complejos. Los medicamentos usualmente son una mezcla de químicos hechos de los materiales primordiales y fuentes de medicamentos. Dependiendo de la fuente de donde se crea el medicamento, los medicamentos pueden ser categorizados como naturales, sintéticos o semi-sintéticos.6
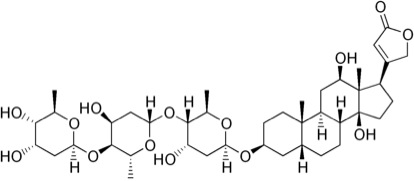
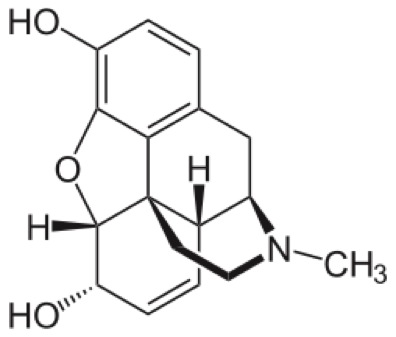
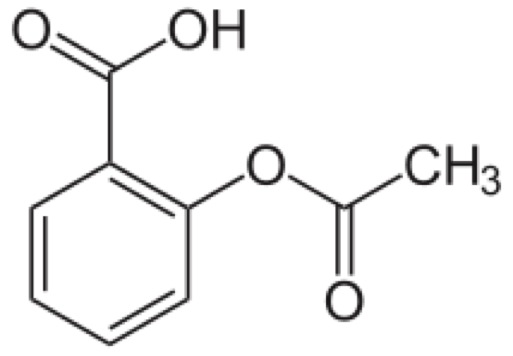
Los fármacos naturales están hechos de compuestos encontrados en la naturaleza. Las fuentes más prevalentes de fármacos naturales son las plantas. La rama de la ciencia que estudia la relación entre la gente y plantas medicinales se conoce como etnobotánica medicinal. Algunos ejemplos de medicinas que vienen de plantas son morfina (del opio), digoxina (de la flor Digitalis lanata) y aspirina (de la corteza del sauce). Fuentes menos prevalentes de medicamentos incluyen a animales, microbios y minerales.6
De izquierda a derecha: amapola de opio, Digitalis lanata, árbol de sauce
De izquierda a derecha: Estructura de morfina, estructura de ácido acetilsalisílico (aspirina)
Los fármacos sintéticos vienen de materiales fundamentales que no se encuentran en la naturaleza. En vez, son producidos por el hombre de piezas químicas más pequeñas.6 Un ejemplo de un medicamento sintético es el fármaco experimental de anti-malaria, arterolane.7
Los fármacos semi-sintéticos no son completamente naturales ni completamente sintéticos: son híbridos. Los medicamentos semi-sintéticos generalmente son generados al convertir materiales primordiales que vienen de fuentes naturales a productos finales mediante reacciones químicas. Ejemplos de medicamentos semi-sintéticos incluyen el antibiótico penicilina y el medicamento quimioterápico paclitaxel. Para hacer el medicamento quimioterápico paclitaxel, se extrae 10-desacetilbacatina de agujas de tejo y se pasa por un proceso llamado síntesis de 4to nivel.6

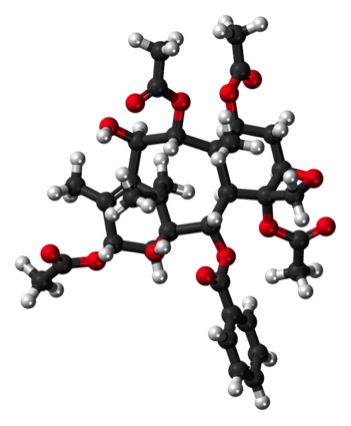
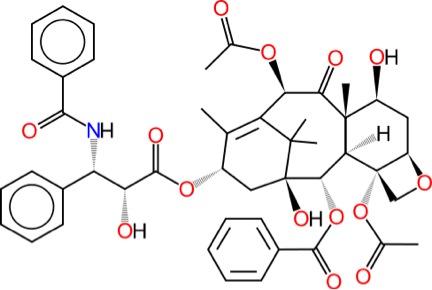
De derecha a izquierda: Agujas de tejo, estructura de 10-desacetilbacatina, estructura de paclitaxel.
En general, el descubrimiento de fármacos naturales envuelve cribar y identificar compuestos activos en extractos creados de plantas, animales, microbios y minerales. El desarrollo de fármacos sintéticos envuelve producir compuestos químicos puros y aislados con la ayuda de investigación computarizada y colecciones grandes de químicos. La meta del descubrimiento de ambos tipos de fármacos es identificar candidatos: químicos que puedan tener efectos terapéuticos y puedan tratar condiciones médicas, incluyendo cáncer, infecciones, presión alta, enfermedades del sistema nervioso y enfermedades metabólicas.6
Pros y Contras de Fármacos Naturales y Sintéticos
Ventajas de fuentes naturales para medicamentos:6
- Más diversidad y novedad estructural en comparación a compuestos sintéticos.
- Muchos químicos naturales pueden interactuar con proteínas y otras moléculas biológicas.
- Estructuras más complejas que moléculas sintéticas. Esta complejidad permite ser más selectiva al atarse a su objetivo.
Desventajas de usar fuentes naturales:6
- Toma más tiempo
- Más costoso
- Menos sustentable
- Compuestos químicos naturales pueden funcionar diferente de lo que se espera una vez se extrae de su fuente.
Ventajas de usar fármacos sintéticos 6
- Toma menos tiempo
- Cuesta menos
- Más sustentable
Desventaja de uasr fuentes sintéticas de medicamentos 6
- Tienden a tener menor efecto terapéutico
- Muchos fármacos sintéticos causan efectos secundarios inacceptables.
Aprenda más sobre los efectos secundarios de los tratamientos de cáncer.
Ejemplos de Medicamentos de Cáncer
Metotrexato (MTX)
- Categoría
- Sintético
- Mecanismo de acción
- Anti-folato - Bloquea el crecimiento celular de cáncer al prevenir que las células cancerosas usen folato para hacer ácidos nucléicos (ADN y ARN)8
- Compite con folato para enlazarse a la enzima dihidrofolato reductasa, previniendo que dihidrofolato se convierta en tetrahidrofolato (un ingrediente esencial en el reparamiento y síntesis de ADN).9
- Desarrollo
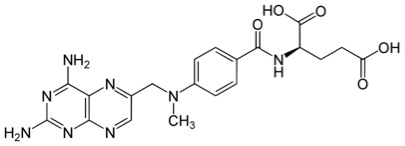
Estructura de metotrexato
Aprenda más sobre metotrexato.
Aprenda sobre la resistencia de cánceres a metotrexato.
Sorafenib (Nexavar)
- Categoría
- Sintético 11
- Mecanismo de acción
- Desarrollo
- Hay varios mecanismos sintéticos, pero el método más aceptado envuelve la reacción de isocianato con anilina usando diclometano como reactivo. Esto da un rindimiento de 92%.11
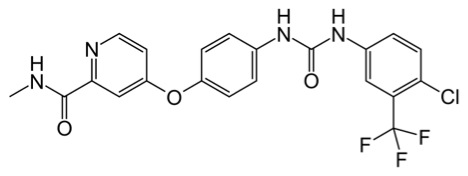
Estructura de sorafenib (Nexavar)
Vinblastina
- Categoría
- Se encuentra naturalmente y también es producido sintéticamente.13
- La extracción es costosa así que solo es sustentable sintéticamente.
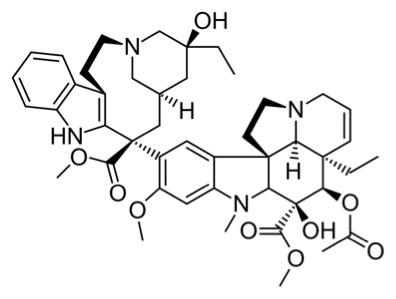
- Vinblastina es un alkaloide encontrado en la vinca de Madagascar (Catharanthus roseus aka Vinca rosea)13
- Usada para tratar linfomas, cáncer testicular y cáncer de seno14
- Mecanis de acción
- Detiene el crecimiento tumoral al interrumpir la formación de microtúbulos e inhibiendo división celular. Los microtúbulos son parte del citoesqueleto y son importante para la división celular. Vinblastina ata a los bloques fundamentales usados para crear los microtúbulos y previenen que se formen cadenas largas.13
- Desarrollo
De izquierda a derecha: vinca de Madagascar, estructura de vinblastina
Buscando Medicamentos Posibles
Fármacos Naturales
Durante las primeras etapas del proceso de descubrimiento y desarrollo de un fármaco, los científicos tienen que escoger los químicos más prometedores (líderes o candidatos) para avanzar el estudio. Para hacer esto aislan y purifican los compuestos líderes de sus fuentes naturales. Los métodos y equipo envueltos en este paso dependen de la estructura, estabilidad y cantidad del compuesto necesitado. En el caso de penicilina, la cromatografía y secar en frío son las dos técnicas que se usan.6
Para encontrar los candidatos más prometedores, los científicos tienen que buscar compuestos para ser estudiados a mayor profundidad. Para buscar eficientemente candidatos, típicamente se usa el cribado de alto rendimiento (HTS). En HTS, máquinas prueban miles de químicos contra objetivos específicos. HTS se ha convertido en el método estándar de conducir millones de pruebas que ayudan a identificar los efectos medicamentos posibles en las vías biológicas.6
Después de que las pruebas bioquímicas y farmacológicas apropiadas han sido conducidas, los científicos achican la lista para incluir solo los mejores compuestos que tengan la habilidad de reaccionar con moléculas específicas de la manera deseada. En esta etapa del proceso de descubrimiento de fármacos, la mayoría de los compuestos no son suficientemente selectivos hacia la molécula deseada. Para poder incrementar la selectividad, químicos medicinales alteran la estructura de los compuestos de acuerdo a lo que ellos prediquen que sea más efectivo. Si las alteraciones mejoran la selectividad, los candidatos pueden pasar a la etapa in vitro y in vivo de las pruebas. 6
Fármacos Sintéticos
Las etapas generales del descubrimiento de fármacos sintéticos en muy similar al proceso de descubrimiento natural. La diferencia clave es que el origen de los compuestos líderes. En el descubrimiento de fármacos naturales, los compuestos vienen de fuentes naturales mientras que en el descubrimiento de fármacos sintéticos, los compuestos típicamente son generados en laboratorios mediante química combinacional, una técnica por la cual millones de moléculas son creadas de partes más pequeñas.
La química combinacional es usada en laboratorios para crear un gran número de moléculas deseadas. Este método es una manera eficiente de crear muchos químicos nuevos, pero genera moléculas que son estructuralmente menos complejas que si fueran naturales. Síntesis de modelo de ADN es una técnica de síntesis desarrollada recientemente que le permite a los investigadores escanear más eficientemente por compuestos que tengan interacciones deseadas con otras moléculas biológicas. También puede producir moléculas que quizás no se pudiesen haber hecho mediante técnicas estándares. En este momento, el descubrimiento de fármacos sintéticos tiene tasas de éxito más bajas mediante HTS porque los productos no son tan diversos como aquellos encontrados naturalmente.6
Examinando Con Precausión los Fármacos Posibles
Después de seleccionar exitosamente y escanear por compuestos líderes, los científicos le tienen que hacer pruebas de seguridad para ver si deben continuar en el proceso de desarrollo. Específicamente, es importante saber cómo el medicamento es absorbido, distribuido, metaboilizado y excretado (ADME). La prueba ADME provee información sobre que le pasa al medicamento cuando está dentro del cuerpo, un un campo de estudio llamado farmacocinética.16 Compuestos prometedores tienen que ser no-tóxicos y capaz de ser absorbido en los vasos sanguíneos, ditribuido a su objetivo, metabolizado efectivamente y excretado del cuerpo.17
diagrama ADME
Optimización y Pruebas Pre-Clínicas
Optimización de compuestos líderes
El propósito de la optimización de los compuestos líderes es disminuir los efectos negativos asociados con los compuestos y hacerlos más efectivos y selectivos. Los científicos optimizan los compuestos líderes al cambiar sus estructuras y probando estas variaciones (análogos). Si la optimización es exitosa, los compuestos líderes pueden continuar el proceso de desarrollo del fármaco donde se convierten en posibles candidatos para medicamentos.17
Escaneo de seguridad
Esta etapa en el proceso de descubrimiento y desarrollo de medicamentos tiene varias metas. Los científicos tienen que determinar si el candidato a ser medicamento es saludable para pruebas humanas. También tienen que saber cómo exactamente funciona el medicamento y determinar maneras efectivas y eficientes de producir cantidades grandes del medicamento candidato - un proceso necesario si el medicamento candidato continuará a la etapa de ensayo clínico. Medicamentos candidatos que pasen las pruebas de seguridad son elegibles para solicitudes a ensayos clínicos.17
Solicitudes para Nuevo Medicamento Investigacional (IND)

El propósito de esta etapa en el proceso de descubrimiento y desarrollo de medicamentos es determinar si el candidato a ser un fármaco puede ser usado en ensayos clínicos. La FDA y el Institutional Review Board (IRB) tienen que aprobar el IND para que el ensayo clínico pueda comenzar. La FDA revisa todo el trabajo anterior para asegurarse que los ensayos clínicos serán razonablemente seguros y no habrán riesgos poco razonables. La IRB revisa los planes para los ensayos clínicos que detallan cómo serán corridos estos ensayos, que instituciones, investigadores y doctores estarán involucrados y asegurarse que los pacientes estén informados correctamente. Si la solicitud para IND es aprovada, el medicamento candidato continúa hacia los ensayos clínicos.17
Ensayos Clínicos
Después que las pruebas de laboratorio y en animales han sido completadas exitosamente, los medicamentos potenciales son entonces pasados por una serie de ensayos en voluntarios humanos. Medicamentos que funcionan bien en otros animales quizás no funcionen en humanos o pueden tener efectos secundarios que surgen en humanos pero no en otros animales. Estos ensayos clínicos son compuestos de varios pasos, o fases, descritos debajo.
Fase 0
Esta fase es designada a eliminar ciertos medicamentos candidatos que son considerados inefectivos. Esto es hecho mediante "microdosificación" - cantidades pequeñas de un medicamento. Esto se le da a varios voluntarios y se analizan sus efectos. Los medicamentos que pasen continúan a la fase 1. No todos los medicamentos candidatos pasan por fase 0.17
Fase I
Esta fase es designada para determinar si el medicamento candidato es saludable para humanos. A un grupo pequeño de voluntarios (entre 20-100 personas) se les da el medicamento candidato y los efectos son analizados. Los científicos estudian la farmacocinéticas (ADME, efectos secundarios, efectos deseados, dosificaciones saludables, etc.) durante esta etapa. Los medicamentos candidatos que pasen esta etapa continúan a la segunda fase.17
Fase II
Esta fase está diseñada para determinar la efectividad del medicamento candidato en un grupo de pacientes más grande (100-500 personas) que tienen la enfermedad que está siendo estudiada. Los efectos secundarios, mecanismo de acción, eficacia y la dosificación óptima del medicamento candidato son analizados. Los candidatos que pasen continúan hacia la última etapa.17
Fase III
Esta fase es diseñada para determinar la seguridad, eficacia y ventajas contra desventajas del medicamento en un grupo mucho más grande (1,000-5,000 personas). La información conseguida en esta fase será utilizada para crear las direcciones de uso del medicamento (riesgos, posibles interacciones con otros medicamentos, etc.). Los medicamentos candidatos que pasen esta fase serán elegibles para una Solicitud de Nuevo Medicamento (NDA).17
Solicitud de Nuevo Medicamento (NDA)
Después de la fase III de los ensayos clínicos, la compañía patrocinadora analiza toda la información recogida de los ensayos clínicos para determinar si el medicamento candidato es suficiente saludable y efectivo para continuar hacia la próxima etapa: una NDA para aprobación por la FDA para vender el medicamento. La NDA es una colección de información que incluye estudios del medicamento, propuestas de fabricación y posibles etiquetas para el medicamento. La FDA, en conjunto con expertos nombrados por la FDA, revisan la información para determinar si el medicamento puede ser aprobado como una nueva medicina. Hay tres posibles resultados:
- La FDA puede aprobar el medicamento candidato como una medicina nueva.
- La FDA le puede pedir a la compañía patrocinadora más información y/o estudios antes de tomar una decisión.
- El medicamento candidato puede ser denegado.
Posterior a la Aprobación: Producción, Fase IV e Investigación Continuada
Si la FDA aprueba el medicamento candidato como una medicina nueva, la compañía patrocinadora puede entonces empezar el proceso complicado y costoso de producir el medicamento a gran escala. También tienen que cumplir con las directrices de la FDA para Prácticas Propias de Manufactura (GMP). Fase IV, la vigilancia de los efectos del medicamento en los pacientes a largo plazo, comienza tan pronto el medicamento ha sido administrado a pacientes en un ambiente fuera de los ensayos. Periódicamente, la compañía patrocinadora del medicamento tiene que someter reportes a la FDA detallando la eficiencia y seguridad de la medicina y cualquier tipo de preocupación reportada.18
Aspecto Financiero del Desarrollo y Venta del Medicamento
La mayoría de los fármacos posibles que son identificados temprano en el proceso de desubrimiento y desarrollo no llegan hasta el fin del proceso. El proceso entero de descubrir y desarrollar un medicamento es extremadamente costoso y puede durar por más de una década. De acuerdo a un estudio de 2014 conducido por el Centro de Estudio del Desarrollo de Fármacos de Tufts, desarrollar una medicina de prescripción nueva cuesta aproximadamente $2.558 mil millones. Aproximadamente $1.395 mil millones de esto son para cubrir los costos del presupuesto, mientras el resto de los $1.163 mil millones son para cubrir el costo de tiempo (el dinero que los inversionistas tienen que poner en lo que el medicamento está siendo producido). Este costo del 2014 representa un incremento de 145% del costo reportado en el 2013. Los siguientes factores son posibles explicaciones de por qué incrementó el costo:
- Los ensayos clínicos son más grandes y complejos
- Mayor tasa de fracaso de los medicamentos probados en humanos.
- Cambios de protocolo para incluir información de la evaluación de tecnologías de salud,19, 20
Cuando un medicamento se ve prometedor, la compañía típicamente solicitará para un patente para proteger su producto de la competencia. En los Estados Unidos, patentes de fármacos duran 20 años. Como las compañías usualmente solicitan por los patentes varios años antes de que esté listo el medicamento, puede que solo tengan prácticamente una década cubierta por el patente para cubrir sus costos y empezar a generar dinero. El costo tan extremadamente caro asociado con llevar un medicamento del laboratorio a la gente es una de las razones por la cual los medicamentos frecuentemente son caros.
Aprenda más sobre el Centro de Estudio de Desarrollo de Fármacos de Tufts
- 1ab Petrovska BB. Historical review of medicinal plants' usage. Pharmacogn Rev. 2012 Jan;6(11):1-5. [PUBMED]
- 2ab Historical Background to Drug Discovery. UGA Center for Drug Discovery. [http://www.uga-cdd.org/background.php]
- 3 Maehle AH, Prull CR, Halliwell RF. The emergence of the drug receptor theory. Nat Rev Drug Discov. 2002 Aug;1(8):637-41. [PUBMED]
- 4 Pereira DA, Williams JA. Origin and evolution of high throughput screening. Br J Pharmacol. 2007 Sep;152(1):53-61. Epub 2007 Jul 2. [PUBMED]
- 5 Pandeya SN, Thakkar D. Combinatorial chemistry: A novel method in drug discovery and its application. Indian Journal of Chemistry. Vol. 44B, Feb 2005, pp. 335-348. [http://nopr.niscair.res.in/bitstream/123456789/8939/1/IJCB%2044B(2)%20335-348.pdf]
- 6abcdefghijklm Lahlou M. The Success of Natural Products in Drug Discovery. Pharmacology & Pharmacy, 2014, 4, 17-31.
- 7 Valecha N, Looareesuwan S, Martensson A, Abdulla SM, Krudsood S, Tangpukdee N, Mohanty S, Mishra SK, Tyagi PK, Sharma SK, Moehrle J, Gautam A, Roy A, Paliwal JK, Kothari M, Saha N, Dash AP, Bjorkman A. Arterolane, a new synthetic trioxolane for treatment of uncomplicated Plasmodium falciparum malaria: a phase II, multicenter, randomized, dose-finding clinical trial. Clin Infect Dis. 2010 Sep 15;51(6):684-91. [PUBMED]
- 8 Methotrexate. American Cancer Society. [http://www.cancer.org/treatment/treatmentsandsideeffects/guidetocancerdrugs/methotrexate]
- 9ab Skubisz MM, Tong S. Of leaves and butterflies: how methotrexate came to be the savior of women. Obstet Gynecol. 2011 Nov;118(5):1169-73. [PUBMED]
- 10 WHO Model List of Essential Medicines. [http://apps.who.int/iris/bitstream/10665/93142/1/EML_18_eng.pdf?ua=1]
- 11ab Zhang L, Xia W, Wang B, Luo Y, Lu W. Convenient Synthesis of Sorafenib and its Derivatives. Synthetic Communications, Vol 41 Issue 21, 2011.
- 12ab Sorafenib tosylate. National Cancer Institute. [http://www.cancer.gov/drugdictionary?cdrid=299013]
- 13abcd Ishikawa H, Colby DA, Seto S, Va P, Tam A, Kakei H, Rayl TJ, Hwang I, Boger DL. Total synthesis of vinblastine, vincristine, related natural products, and key structural analogues. J Am Chem Soc. 2009 Apr 8;131(13):4904-16. [PUBMED]
- 14ab Vinblastine. CancerQuest. [http://www.cancerquest.org/patients/drug-reference/vinblastine]
- 15 Dr. Robert Laing Noble. The Canadian Medical Hall of Fame. [http://cdnmedhall.org/dr-robert-laing-noble]
- 16 Eddershaw PJ, Beresford AP, Bayliss MK. ADME/PK as part of a rational approach to drug discovery. Drug Discov Today. 2000 Sep;5(9):409-414. [PUBMED]
- 17abcdefgh Drug Discovery and Development: Understanding the R&D Process. Innovation.org. [http://www.innovation.org/drug_discovery/objects/pdf/RD_Brochure.pdf]
- 18 Suvarna V. Phase IV of Drug Development. Perspect Clin Res. 2010 Apr;1(2):57-60. [PUBMED]
- 19 Herper, Matthew. How Much Does Pharmaceutical Innovation Cost? A Look At 100 Companies. Forbes. [http://www.forbes.com/sites/matthewherper/2013/08/11/the-cost-of-inventing-a-new-drug-98-companies-ranked/]
- 20 Cost of Developing a New Drug. Tufts Center for the Study of Drug Development. Tufts University. [http://csdd.tufts.edu/files/uploads/Tufts_CSDD_briefing_on_RD_cost_study_-_Nov_18,_2014..pdf]