Erlotinib
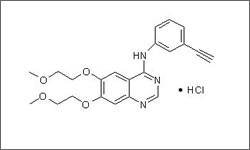
Brand name:
Tarceva®
IUPAC:
N-(3-ethynylphenyl)-6,7-bis(2-methoxyethoxy) quinazolin-4-amine
FDA approval:
Yes
Usage:
El FDA ha aprobado erlotinib para tratar:
Localmente avanzado o metastásico de células no pequeñas de cáncer de pulmón (tras el fracaso de al menos un tratamiento previo). Cáncer de páncreas localmente avanzado, metastásico o no resecable (en combinación con gemcitabina).
Mechanism:
Erlotinib es un inhibidor de tirosina quinasa asociada con el receptor de factor del crecimiento epidermal humano. Por inhibir la función de esto receptor, que es sobreexpresado en células cancerosas, erlotinib bloquea proliferación de células y promueve muerte de células cancerosas.
Side effects:
Efectos secundarios incluyen:
Anemia y trombocitopenia (nivels bajos de glóbulos blancos y rojos), diarreah, anorexia, mareos, vomito, tos, dificultad para respirar, irritación de los ojos
Contraindications:
Reacciones adversos severos potenciales pueden incluir toxicidad de los pulmones (incluyendo neumonía, enfermedad pulmonar intersticial y el síndrome de distrés respiratorio agudo), infarto de miocardio, hemorragia o insuficiencia hepática. A causa de la potencial para dañar el feto, mujeres no deben embarazarse durante o inmediatmente después del tratamiento. Mujers que ya son embarazadas deben ser avisados de este riesgo al feto en desarrollo. Madres nuevas no deben amamantar durante el tratamiento por es posible que la droga puede pasar al leche.
