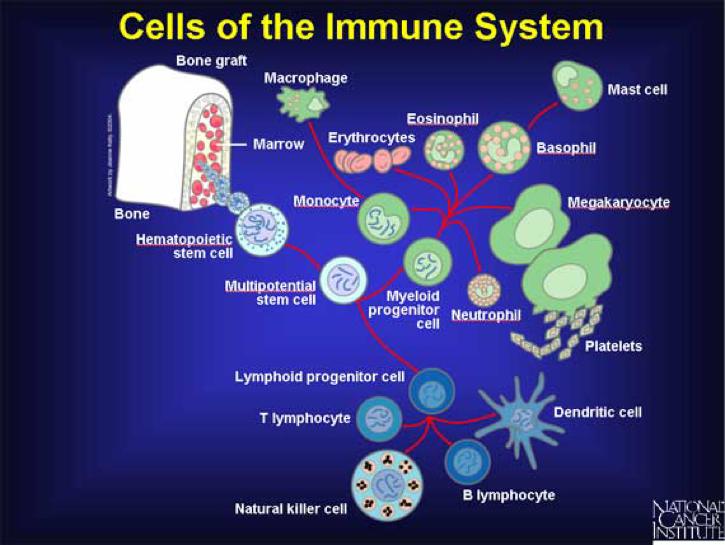
¡Gracias a tu sistema inmune, tú ya tienes el poder de combatir el cáncer dentro de tí! Aunque el sistema inmune usualmente sea asocia con la protección en contra de virus, bacterias y otros organismos que causan enfermedades, realmente tiene un rol muy importante en ayudar a combatir el cáncer y poder detectar y destruir a células cancerígenas.
Una de las funciones más importantes del sistema inmune es poder reconocer objetos foráneos (virus, bacteria, parásitos y todo lo que no se supone que esté dentro de tu cuerpo) y destruirlos. Para hacer esto, las células inmunes se guían con las superficies de los cuerpos extraños. Ya que las células cancerígenas son anormales, las células inmunes las consideran como objetos foráneos. Por ende, el sistema inmune logra destruir a las células del cáncer.
Aprenda más en nuestra sección sobre el sistema inmune
Temas a ser discutidos en esta página:
- ¿Por qué se contrae el cáncer?
- Batallas entre el sistema inmune y las células cancerígenas
- Cómo contrarrestar las defensas de las células cancerígenas
Desafortunadamente, el sistema inmune también participa en el desarrollo de cáncer. Las células no actúan con consciencia, pues solamente siguen las señales celulares que se emiten. Aprenda más sobre esto aquí:
¿Por qué se contrae el cáncer?
Una de las funciones más importantes del sistema inmune cuenta con del reconocimiento de objetos foráneos (viruses, bacteria, parásitos y todo lo que no se supone que esté dentro de tu cuerpo) y su destrucción. Las moléculas que se encuentran sobre la superficie de estos objetos facilitan su detección. Ya que las células cancerígenas son anormales, el sistema inmune las considera como objetos foráneos. Las células inmunes detectan la presencia de moléculas pequeñas que se adhieren a tumores (conocidas como antígenos específicos a tumores o antígenos asociados a tumores). Al ubicar a estas células, el sistema inmune entonces las destruyen.
Nota: Un antígeno se puede definir como cualquier objeto que el sistema inmune logra reconocer, pues es un término general. Los antígenos pueden ser proteínas, azúcares, lípidos, ácidos nucleicos o moléculas híbridas. La mayoría son proteínas.
¿Si el sistema inmune tiene la habilidad de reconocer y matar a células cancerígenas, por qué las personas contraen el cáncer?
Se presume que el sistema inmune logra detectar a la mayoría de los cánceres en sus etapas tempranas, y posteriormente las elimina. Los cánceres que logran sobrevivir son aquellos que se resisten al sistema inmune. Existen varios mecanismos que las células cancerígenas utilizan para evitar ser reconocidas y destruidas. Éstas incluyen:
- Las células cancerígenas provienen de células normales. Como el cáncer surge de las células comunes de la persona, es más difícil para el sistema inmune reconocer la célula como un invasor.
- Las células cancerígenas con más objetivos moleculares se detectan con más facilidad. Aunque esto parezca ser oportuno ya que causa que tumor se encoja en tamaño, con el tiempo, las únicas células que quedan son aquellas que carecen de estos objetivos moleculares. Estas células son las que tienen más probabilidad de sobrevivir y por ende tienden a dominar. Como resultado, se crea una cierta resistencia al sistema inmune. Este proceso se asemeja a un jardín con malas hierbas. Las hierbas resistentes al herbicida sobreviven, crecen y se esparcen por el jardín, por lo cual el herbicida deja de funcionar.
- Las células cancerígenas logran apoderarse de los mecanismos que controlan el sistema inmune. Para regular al sistema inmune, existen varios mecanismos (como un botón que enciende y apaga) que monitorean la actividad de las células inmune. Algunas células cancerígenas desactivan estos mecanismos de control, apagando al sistema inmune en el área del tumor. Actualmente se desarrollan tratamientos nuevos para contrarrestar este proceso.
- Las células cancerígenas logran evadir al sistema inmune al producir menos señales celulares que las hacen detectables. En condiciones normales, el sistema inmune utiliza las proteínas que se encuentran sobre la superficie de las a células cancerígenas como guías para la detección de las mismas. Por ende, si la célula cancerígena se deshace de esta proteína o la esconde, el sistema inmune no logra detectarla.1, 2, 3
Batallas entre el sistema inmune y las células cancerígenas
La batalla entre el sistema inmune y el cáncer es compleja y puede durar muchos años. Comúnmente, el sistema inmune logra eliminar a la mayoría de los cánceres en sus etapas tempranas, antes de que haya cualquier evidencia de su presencia. Solamente los cánceres que se resisten al sistema inmune son los que crecen y representan un peligro para el paciente.
Cómo el sistema inmune mata a células cancerígenas
Las células del sistema inmunológico se organizan según sus funciones para trabajar en conjunto al generar una reacción inmune.
Las células NK (del inglés, 'Natural Killer' - asesina natural) tienen la habilidad de detectar la presencia de ciertas proteínas que se encuentran sobre la superficie del tumor. Estas células inmunológicas producen proteínas que perforan las membranas de las células tumorígenas, causando su muerte.
Otras células, los macrófagos y las células dendríticas también participan al producir proteínas de señalización celular (citoquinas) que reclutan y activan a las células-T (también conocidas como linfocitos-T). La activación de los linfocitos-T puede causar la muerte de las células de cáncer de manera directa, o el 'reclutamiento' de otro tipo de célula inmune: las células-B. Estas se encargan de la producción de anticuerpos que se adhieren a las células cancerígenas, intensificando las reacciones inmunes. Como resultado, las células cancerígenas se encuentran vulnerables y propensas a morir.4, 5, 6, 7
¿Cómo puede una célula cancerosa desactivar al sistema inmune?
Para reiterar, el sistema inmune es bastante complejo y potente. Por lo tanto, no sorprende que existan mecanismos regulatorios que lo desactivan cuando no se requiere su actividad. El ligando de muerte programada 1 (PD-L1) funciona como una molécula regulatoria del sistema inmunológico. Es una proteína que normalmente se encuentra en células inmunes llamadas macrófagos. El PD-L1 se adhiere a otra proteína, la PD-1, que se encuentra sobre la superficie de las células-T. Cuando estas dos proteínas se unen, las células-T detienen su.
Si una célula cancerígena lleva consigo mismo un PD-L1 sobre su superficie, al entrar en contacto con ellas, los linfocitos-T se pueden desactivar, facilitando la supervivencia de las mismas.
Una señal adicional, en la cual participan las proteínas CTLA-4 y B7-1, también puede provocar la suspensión de la actividad de los linfocitos-T. Al igual que la PD-1, la CTLA-4 se encuentra sobre la superficie de los linfocitos-T. Cuando la CTLA-4 se adhiere a la B7-1, la célula-T se desactiva.8, 9, 10
¿Cómo se contrarrestan los mecanismos de defensa que poseen las células cancerígenas?
Muchos investigadores buscan desarrollar un tratamiento que estimule la actividad del sistema inmune de los pacientes de cáncer. Los medicamentos que se enfocan en los mecanismos de evasión inmunológica han producido resultados muy exitosos y su investigación continúa el día de hoy.
Los tratamientos que estimulan la actividad del sistema inmune se clasifican en las siguientes categorías:
1. Activación inmune generalizada
Existen varias proteínas que pueden impulsar la actividad general del sistema inmune. Las señales provenientes de estas proteínas (citoquinas) pasan de célula a célula, aumentando la actividad inmunológica en el cuerpo. Este proceso no es propio de una sola enfermedad o de un tipo de cáncer. La idea detrás del uso de estas señales celulares en el tratamiento del cáncer es que el sistema inmune puede matar al cáncer con más facilidad cuando se encuentra activo. Estas señales le ponen al sistema inmunológico en alerta. Por ejemplo, el interferon-alfa (α-IFN) y la interleucina 2 (IL-2) son citoqunas que estimulan al sistema inmune. Estas proteínas se pueden elaborar en el laboratorio y su uso en el tratamiento de ciertos tipos de cáncer está aprobado.11, 12, 13, 14
2. Bloqueadores de Puntos de Control
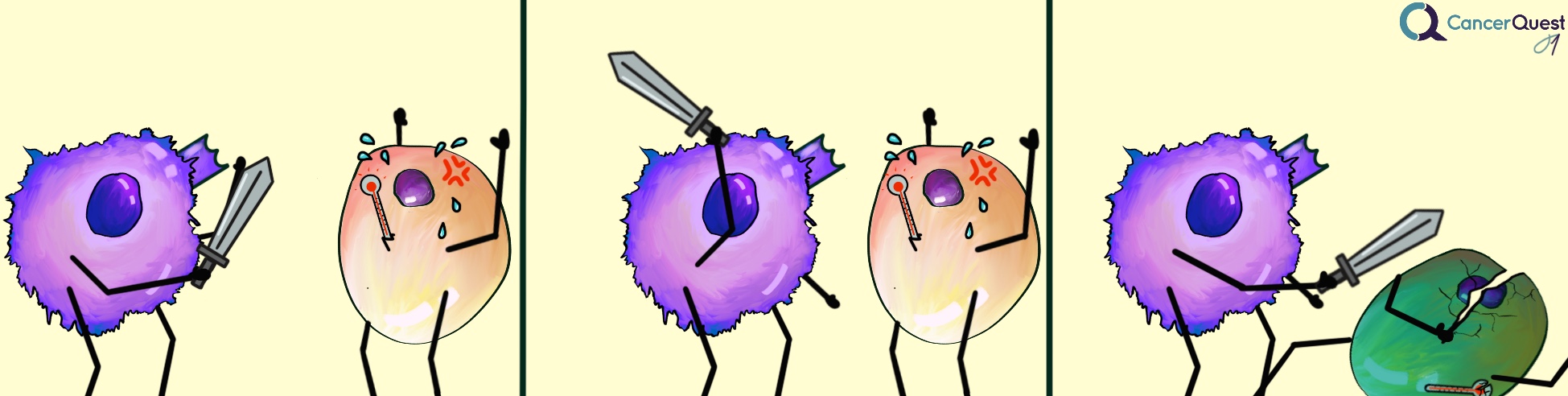
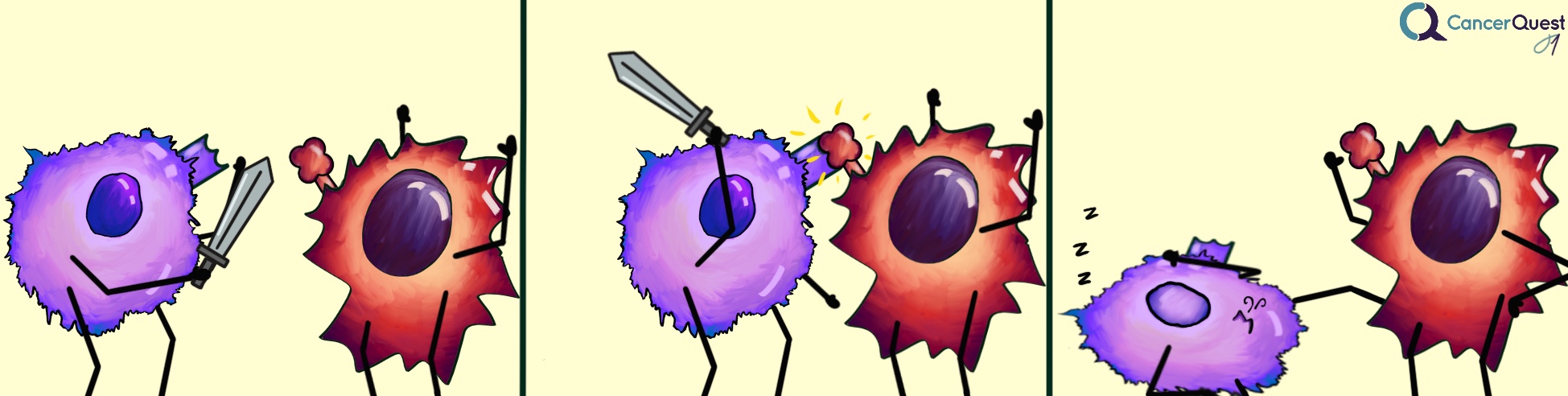

Estos medicamentos tienen la función de re-activar a las células inmunológicas que se encuentran desactivadas como resultado de ciertas interacciones entre proteínas.
Una de las primeras inmunoterapias que aprobó la FDA para su uso en el tratamiento del cáncer es el ipilimumab (conocida como Yervoy®). El medicamento en realidad es un anticuerpo, un tipo de proteína que se adhiere a ciertos tipos de objetivos moleculares/celulares para neutralizarlos o para indicar que tal molécula/célula se debe eliminar. El Yervoy ayuda prolongar la respuesta inmune contra el cáncer al enlazarse y al detener la actividad de la CTLA-4, manteniendo la continuidad de la reacción inmunológica.

El uso del Yervoy® está aprobado para el tratamiento de melanomas ya que los estudios clínicos demostraron que extendía la supervivencia de los pacientes.15 Actualmente, el Yervoy® está bajo investigación en algunos estudios clínicos que evalúan su eficacia en contra del cáncer de pulmón, de riñón, y de próstata.16, 17, 18
Pembrolizumab (Keytruda® ) es un fármaco de anticuerpos que se adhiere a la PD-1, bloqueando la interacción entre la PD-1 y el PD-L1. El uso de este tratamiento está aprobado para tratar a pacientes que padecen del melanoma19. La FDA le ha designado el título de 'terapia innovativa' (en inglés, breakthrough therapy) por su uso en el tratamiento de algunos tipos de cáncer pulmonar.20
Aprenda más acerca de los ensayos clínicos del pembrolizumab (Keytruda®) (abre una pantalla nueva)
Otro tratamiento con anticuerpos anti-PD-1, el nivolumab (conocido como Opdivo®), está aprobado en los Estados Unidos para su uso en contra de melanomas y del cáncer pulmonar no-microcítico.21, 22 El Opdivo® funciona igual que el Keytruda®; al bloquear la interacción entre la PD-1 y el PD-L1, las células-T se mantienen activas, aún cuando la célula tumoral lleva consigo mismo el PD-L1 en su superficie. Hoy en día se realizan pruebas clínicas para definir la posibilidad del uso de este medicamento en contra de otros tipos de cáncer.23
Aprenda más acerca de los ensayos clínicos del nivolumab (Opdivo®) (abre una pantalla nueva)
Otra inmunoterapia de anticuerpos, el atezolizumab (nombre comercial, TECENTRIQ®), funciona de manera similar al Opdivo ®, solamente que en este caso, la unión ocurre entre el fármaco y la PD-L1. Los resultados son los mismos: la (re)activación del sistema inmune. El TECENTRIQ® se utiliza como tratamiento de algunos tipos de cánceres de vejiga, pulmón y de seno.
Aprenda más acerca de los ensayos clínicos del atezolizumab (TECENTRIQ®) (abre una pantalla nueva)
La siguiente imagen ilustra la interacción entre una célula cancerígena y linfocito T, un tipo de célula del sistema inmune. Cuando la interacción PD-1/PD-L1 ocurre, la actividad del linfocito T se detiene. Esto puede limitar la habilidad natural que posee el cuerpo de luchar en el cáncer. Los medicamentos de anticuerpos previenen que esto ocurra al adherirse con un componente del complejo molecular. El diagrama presenta a un anticuerpo unido a una PD-1. El Keytruda® y el Opdivo® funcionan mediante este mecanismo.

3. Vacunas contra el cáncer
Otro método que intenta realzar las reacciones inmunológicas en contra del cáncer es el uso de las proteínas propias de las células cancerígenas con fines de estimular al sistema inmune. Para impulsar la respuesta inmune en contra de ciertas células cancerígenas, al paciente se le administra un tratamiento con una o varias proteínas propias de las células del cáncer, creando la oportunidad para que el sistema inmune identifique a estas proteínas como objetivos moleculares. Este método se asemeja a la manera por la cual funcionan las vacunas que previenen enfermedades como las paperas y el sarampión.
Hay muchos estudios en curso que se enfocan en las vacunas en contra del cáncer. Se puede encontrar más información acerca de estas investigaciones en otra de nuestras páginas.
Aprenda más sobre las vacunas de cáncer
4. Terapia de células T con receptores de antígenos quiméricos (del inglés, CAR) se basa en la misma teoría detrás de las vacunas de cáncer, pero con más profundidad. En vez de activar las células con antígenos característicos del cáncer, las células T del mismo paciente se modifican de tal manera que logran atacar a las células cancerígenas con especificidad. La modificación genética de las células T facilitan el reconocimiento de de las proteínas que es encuentran sobre la superficie de las células de cáncer. Los resultados han sido muy exitosos. Un ensayo clínico con linfocitos T-CAR en contra de las células B de la leucemia linfocítica aguda tuvo un 88% de éxito.
En el 12 de julio del año 2017, el comité de consejería de la FDA votó de manera unánime que se debe recomendar la aprobación del uso de la terapia de linfocitos T-CAR en el tratamiento de niños y adultos jóvenes que padecen de una leucemia linfocítica aguda recurrente o resistente al tratamiento convencional. En el 30 de agosto del mismo año, la FDA aprobó el uso del Kymriah®, la primera terapia de genes autorizada por la ley en los Estados Unidos, para tratar a pacientes con edades menores a 25 que sufren de ciertos tipos de leucemia linfocítica aguda de células B. En el mes de octubre del 2017, la FDA aprobó una segunda terapia de células T-CAR. El uso del Yescarta® (axicabtagene ciloleucel) fue aprobado para tratar a algunos pacientes con linfomas difusos de células B grandes. 24

Esta imagen ilustra la estructura general de un receptor de una célula T-CAR. Los sitios de unión de los anticuerpos (Ab) facilitan el reconocimiento de la célula del tumor, induciendo la producción de señales celulares que estimulan al linfocito T, matando a las células cancerígenas.
- 1 Vinay DS, Ryan EP, Pawelec G, Talib WH, Stagg J, Elkord E, Lichtor T, Decker WK, Whelan RL, Kumara HM, Signori E, Honoki K, Georgakilas AG, Amin A, Helferich WG, Boosani CS, Guha G, Ciriolo MR, Chen S, Mohammed SI, Azmi AS, Keith WN, Bilsland A, Bhakta D, Halicka D, Fujii H, Aquilano K, Ashraf SS, Nowsheen S, Yang X, Choi BK, Kwon BS. Immune evasion in cancer: Mechanistic basis and therapeutic strategies. Semin Cancer Biol. 2015 Mar 25. pii: S1044-579X(15)00019-X [Epub ahead of print] [PUBMED]
- 2 Seliger B. Strategies of tumor immune evasion. BioDrugs. 2005;19(6):347-54. [PUBMED]
- 3 Poggi A, Musso A, Dapino I, Zocchi MR. Mechanisms of tumor escape from immune system: role of mesenchymal stromal cells. Immunol Lett. 2014 May-Jun;159(1-2):55-72. Epub 2014 Mar 20. [PUBMED]
- 4 Dunn GP, Old LJ, Schreiber RD. The immunobiology of cancer immunosurveillance and immunoediting. Immunity. 2004 Aug;21(2):137-48. [PUBMED]
- 5 Bindea G, Mlecnik B, Fridman WH, Pagès F, Galon J. Natural immunity to cancer in humans. Curr Opin Immunol. 2010 Apr;22(2):215-22. Epub 2010 Mar 6. [PUBMED]
- 6 Smyth MJ, Dunn GP, Schreiber RD. Cancer immunosurveillance and immunoediting: the roles of immunity in suppressing tumor development and shaping tumor immunogenicity. Adv Immunol. 2006;90:1-50. [PUBMED]
- 7 Bachanova V, Miller JS. NK cells in therapy of cancer. Crit Rev Oncog. 2014;19(1-2):133-41. [PUBMED]
- 8 Swaika A, Hammond WA, Joseph RW. Current state of anti-PD-L1 and anti-PD-1 agents in cancer therapy. Mol Immunol. 2015 Mar 4. pii: S0161-5890(15)00049-8. [Epub ahead of print] [PUBMED]
- 9 Zamarin D, Postow MA. Immune checkpoint modulation: rational design of combination strategies. Pharmacol Ther. 2015 Jun;150:23-32. Epub 2015 Jan 10. [PUBMED]
- 10 Pico de Coaña Y, Choudhury A, Kiessling R. Checkpoint blockade for cancer therapy: revitalizing a suppressed immune system. Trends Mol Med. 2015 Jun 16. [Epub ahead of print] [PUBMED]
- 11 Rizza P, Moretti F, Belardelli F. Recent advances on the immunomodulatory effects of IFN-alpha: implications for cancer immunotherapy and autoimmunity. Autoimmunity. 2010 Apr;43(3):204-9. [PUBMED]
- 12 Ferrantini M, Capone I, Belardelli F. Interferon-alpha and cancer: mechanisms of action and new perspectives of clinical use. Biochimie. 2007 Jun-Jul;89(6-7):884-93. Epub 2007 Apr 21. [PUBMED]
- 13 Rosenberg SA. IL-2: the first effective immunotherapy for human cancer. J Immunol. 2014 Jun 15;192(12):5451-8 [PUBMED]
- 14 Sim GC, Radvanyi L. The IL-2 cytokine family in cancer immunotherapy. Cytokine Growth Factor Rev. 2014 Aug;25(4):377-90. Epub 2014 Aug 1. [PUBMED]
- 15 Hodi FS, O'Day SJ, McDermott DF, Weber RW, Sosman JA, Haanen JB, Gonzalez R, Robert C, Schadendorf D, Hassel JC, Akerley W, van den Eertwegh AJ, Lutzky J, Lorigan P, Vaubel JM, Linette GP, Hogg D, Ottensmeier CH, Lebbé C, Peschel C, Quirt I, Clark JI, Wolchok JD, Weber JS, Tian J, Yellin MJ, Nichol GM, Hoos A, Urba WJ. Improved survival with ipilimumab in patients with metastatic melanoma. N Engl J Med. 2010 Aug 19;363(8):711-23. Epub 2010 Jun 5. [PUBMED]
- 16 Buqué A, Bloy N, Aranda F, Castoldi F, Eggermont A, Cremer I, Fridman WH, Fucikova J, Galon J, Marabelle A, Spisek R, Tartour E, Zitvogel L, Kroemer G, Galluzzi L. Trial Watch: Immunomodulatory monoclonal antibodies for oncological indications. Oncoimmunology. 2015 Mar 2;4(4):e1008814. eCollection 2015. [PUBMED]
- 17 Barbee MS, Ogunniyi A, Horvat TZ, Dang TO. Current Status and Future Directions of the Immune Checkpoint Inhibitors Ipilimumab, Pembrolizumab, and Nivolumab in Oncology. Ann Pharmacother. 2015 May 19. [Epub ahead of print] [PUBMED]
- 18 Villaruz LC, Kalyan A, Zarour H, Socinski MA. Immunotherapy in lung cancer. Transl Lung Cancer Res. 2014 Feb;3(1):2-14. [PUBMED]
- 19 FDA approves Keytruda for advanced melanoma. U.S. Food and Drug Administration website. Published September 4, 2014. Updated September 10, 2014. Accessed September 13, 2014. [http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm412802.htm.]
- 20 Merck Receives FDA Breakthrough Therapy Designation for KEYTRUDA® (pembrolizumab) in Advanced Non-Small Cell Lung Cancer 11/27/2014 [http://www.mercknewsroom.com/news-release/oncology-newsroom/merck-receives-fda-breakthrough-therapy-designation-keytruda-pembroli]
- 21 FDA approves Opdivo for advanced melanoma (FDA News Release) [http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm412802.htm]
- 22 FDA expands approved use of Opdivo to treat lung cancer (FDA News Release) [http://www.fda.gov/newsevents/newsroom/pressannouncements/ucm436534.htm]
- 23 Clinical Trials Search Results for Opdivo® [http://www.cancer.gov/about-cancer/treatment/clinical-trials/search/results?protocolsearchid=14278803]
- 24 FDA approves CAR-T cell therapy to treat adults with certain types of large B-cell lymphoma. FDA website. Accessed 12-1-19 [FDA website]
